苏州近岸蛋白质科技股份有限公司品牌商
15 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
推荐产品
公司新闻/正文
从核苷修饰说起,带你了解mRNA修饰的奥秘
6383 人阅读发布时间:2023-11-30 15:38
mRNA技术的应用领域非常广泛,目前主要用于传染性疾病疫苗、肿瘤免疫治疗、蛋白替代疗法和基因编辑等方面,尤其在肿瘤免疫治疗和传染性疾病疫苗的应用上较为突出。公开数据显示,全球有超过150个mRNA疫苗药物项目正在推进,明确获批及进入临床阶段的也有近百个,其中大约70%为感染性疫苗项目,约30%为肿瘤治疗性疫苗项目。
今年的诺贝尔生理学或医学奖授予了美国科学家卡塔林·卡里科和德鲁·魏斯曼,以表彰他们“他们发现了核苷碱基修饰,从而开发出有效的新冠肺炎mRNA疫苗”。本文总结了mRNA的其他更多重要修饰。
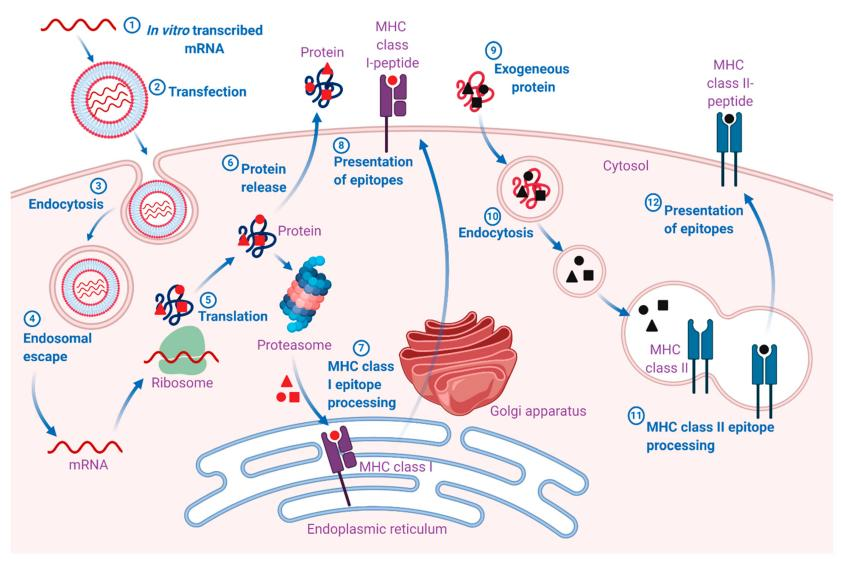
图1 mRNA疫苗的作用机制(Wadhwa A et al. 2020)
体外合成mRNA的修饰
1. 5′端加帽
RNA聚合酶催化RNA的转录合成,这一过程中以DNA为模板;RNA聚合酶作用于DNA模板链的3’端,RNA链从5’端向3’端延伸。转录的同时,mRNA的5’端进行加帽反应,7-甲基鸟嘌呤通过5’-5’三磷酸键与mRNA的5’端连接。根据甲基化修饰的程度不同分为3种帽结构:Cap0、Cap1和Cap2(图3)。
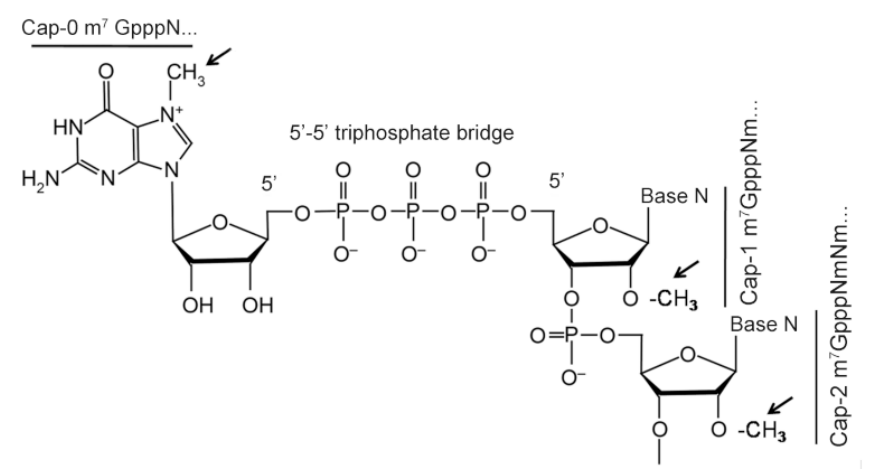
体外合成的RNA需要通过一定的合成过程完成5’端帽结构的添加,从而形成完整的mRNA结构。mRNA的完整性确保了蛋白质的准确翻译,5’-Cap帽结构修饰可以保护mRNA免受5'-外切酶活性降解、有效促进翻译的起始、降低免疫原性。常用的加帽工艺有两类,一类是在IVT结束后,通过牛痘病毒加帽酶和2’-O-甲基转移酶的共同作用,完成Cap1的修饰;一类是在IVT过程中,通过在体系内引入帽类似物,完成帽结构的修饰。两种方式在工艺、结果以及知识产权壁垒等方面各不相同。
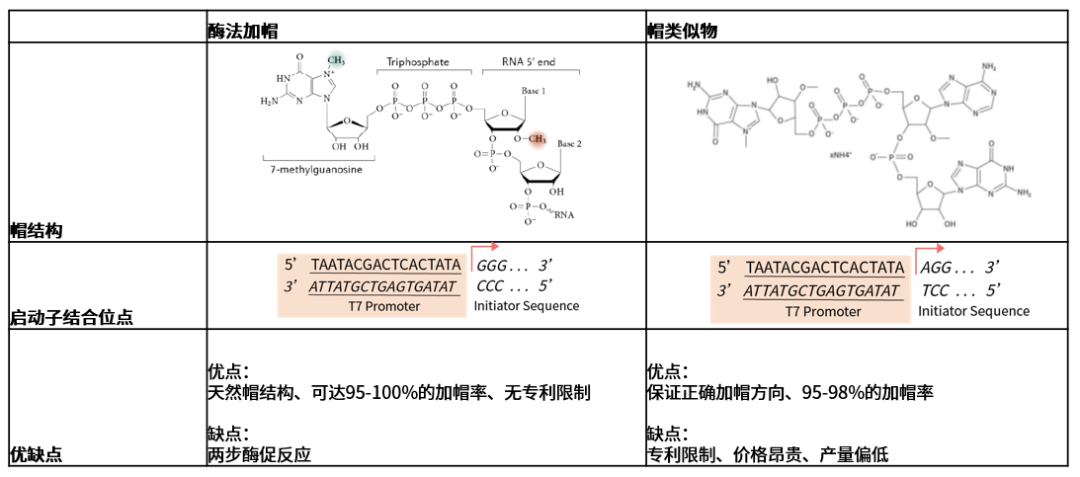
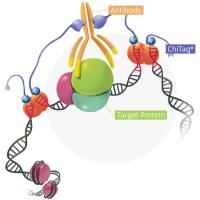
图3 酶法加帽和共转录加帽的比较,图片引用于 Novoprotein Scientific Inc.
酶法加帽过程:在RNA三磷酸酶作用下,mRNA 5’端γ-磷酸基团被去除,生成5’-二磷酸RNA;在鸟苷酸转移酶(guanylyl-transferase)作用下,GTP中的GMP基团与5’-二磷酸 RNA连接;在鸟嘌呤N-7甲基转移酶(guanine-N(7)-methyltransferase)作用下,鸟嘌呤的N7位发生甲基化(甲基供体为S-腺苷甲硫氨酸[SAM]),形成帽结构Cap0(m7GpppNpNp)。而后在2’-O核糖甲基转移酶(2’-O Ribose methyltransferase)作用下,mRNA第一个核苷酸的2’-O位发生甲基化,形成帽结构Cap1(m7Gpppm2’NpNp);mRNA第一个和第二个核苷酸的2’-O位均发生甲基化,形成帽结构Cap2(m7Gpppm2’Npm2’Np)(图5)。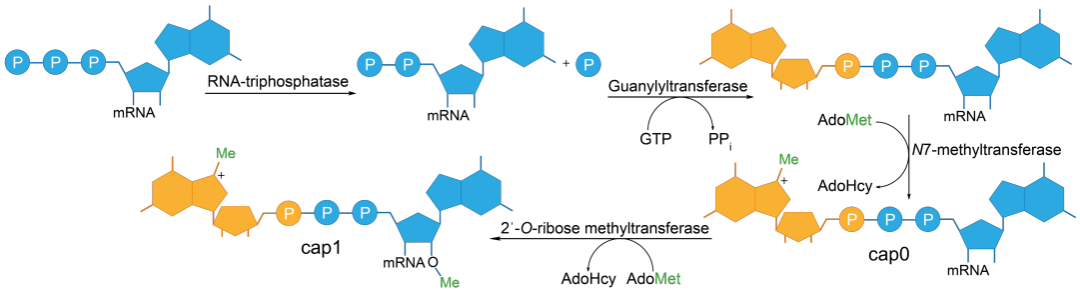
图4 真核生物mRNA中酶促5 '端帽形成的示意图(Muttach F et al. 2017 )
近岸蛋白提供mRNA加帽过程中所需的2种加帽酶:牛痘病毒加帽酶(目录号:GMP-M062、M062)和mRNA Cap2’-O-甲基转移酶(目录号:GMP-M072、M072)及完整试剂盒(目录号:M082)。
2. 3′-端加尾
体外合成mRNA的加尾方式主要有两种:(A)通过Poly(A) Polymerase酶促方式加尾;(B)在模板上引入编码PolyA的序列(图6)。PolyA尾与通过核膜有关,还可防止核酸外切酶降解。这种多聚腺苷酸尾巴很重要,它的长度确定了mRNA在细胞中的存在时间,以及细胞利用mRNA表达蛋白的频率。这种多聚腺苷酸尾巴也是mRNA从细胞核中迁移出去所必需的。早期基于实验证据的假说认为,Poly(A)尾与胞浆中的多聚腺苷结合蛋白(PABPC)促进翻译并阻止mRNA降解(decay),但具体机制并不清楚。最近对Poly(A)尾的作用认识更加丰富:Poly(A)结合蛋白可以促进Poly(A)的去除(即发生脱腺苷化,deadenylation),而当mRNA稳定且高频翻译时,Poly(A)在稳态下的长度远低于预期。此外,翻译延伸的速率会影响脱腺苷化。因此,Poly(A)尾、PABPC、翻译过程和mRNA降解间的相互作用在基因调控中起重要作用。
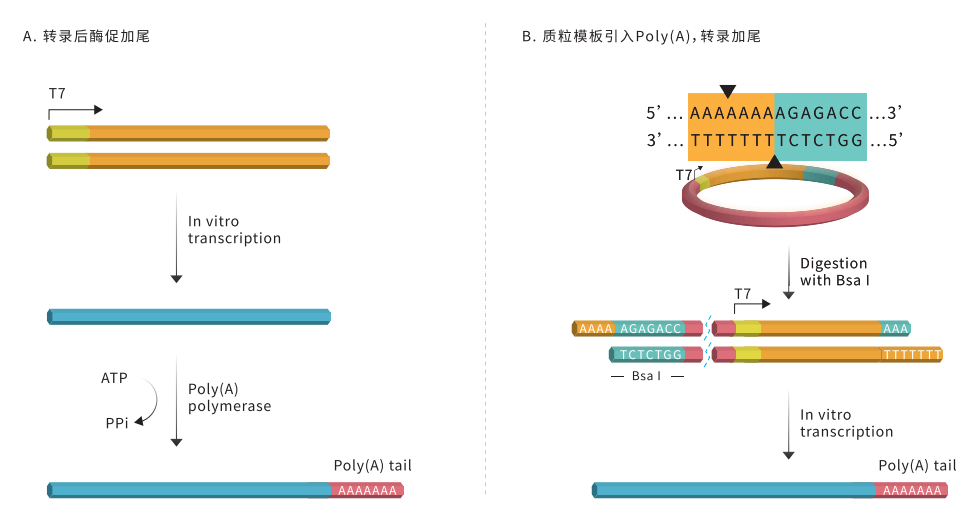
图5 2种加尾方法:(A)转录后酶促加尾;(B)用 Bsal 将模板线性化后进行转录
近岸蛋白提供mRNA加尾过程种所需的加尾酶 E. coli Poly(A) Polymerase (目录号:GMP-M012、M012)。
3. 化学修饰
mRNA中还存在很多化学修饰,有碱基的修饰,也有核糖的修饰。这些修饰可以参与mRNA的剪接、核输出、转录本稳定性和翻译起始等事件,进而调控多种生理及病理过程。迄今为止共鉴定出超过170种RNA化学修饰,mRNA中常见的修饰包括N6-甲基腺苷(N6-Methyl-Adenosine,m6A),5-甲基胞嘧啶(5-methylcytosine,m5C),N1-甲基腺苷(N1-methyladenosine ,m1A),N7-甲基鸟苷(N7-methylguanosine ,m7G),N4-乙酰胞嘧啶(N4-acetylcytosine,ac4C),假尿苷(Ψ),肌苷(I)和核糖甲基化(2'-O-Me),5-甲氧基-尿苷(5-Methoxy-Uridine,5moU)等。其中m6A最为普遍,研究也较多(图7)。
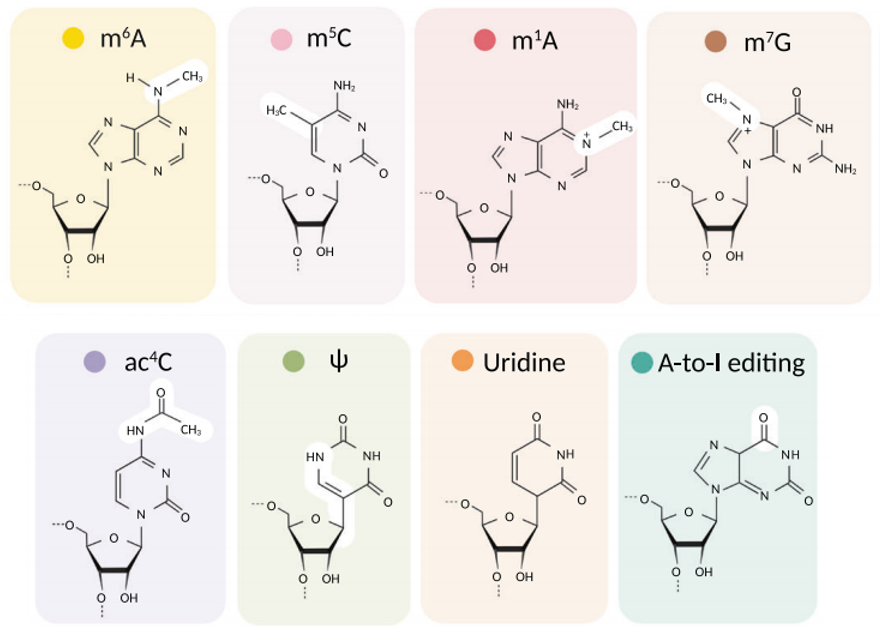
图6 真核生物mRNA的化学修饰成分(Cui L et al. 2022)
近岸蛋白提供mRNA体外合成所需的NTPs (ATP/GTP/CTP/UTP目录号:GMP-S023/S024/S025/S026)和修饰核苷酸pUTP/N1-Me-pUTP(目录号:GMP-S048/GMP-S042)。
所有RNA修饰都可以通过它们的“writers”添加到mRNA上,m6A和m1A修饰可以通过指定的“erasers”去除,因此使这些RNA修饰动态可逆。一些RNA修饰可以被它们各自的解读蛋白识别,从而通过改变靶RNA的产生、运输、功能和代谢改变靶RNA的命运。如下图所示,mRNA不同的位置有着对应的不同化学修饰(图8)。
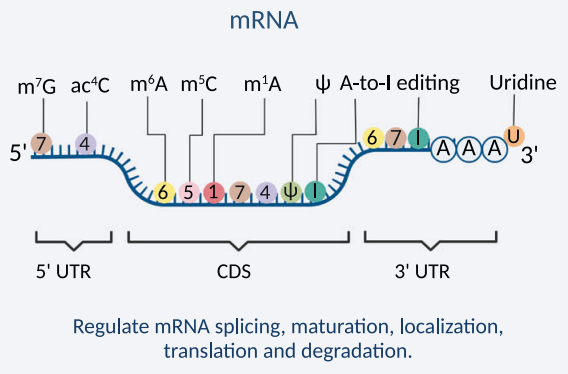
图7 化学修饰在mRNA中的位置(Cui L et al. 2022)
采用修饰核苷酸合成的mRNA可以通过体外转录技术经济高效地大规模生产,并且可以在细胞质中快速瞬时表达,而不会有整合到基因组中的风险。然而,未修饰的合成mRNA不稳定并刺激细胞先天免疫的激活。由于环境RNA酶的高活性,未修饰的合成mRNA在很大程度上存在降解问题。进入细胞后,未修饰的RNA分子会被多种信号受体识别,例如内体Toll样受体、细胞质蛋白激酶R、2′-5′-寡腺苷酸合成酶(OAS)、视黄酸诱导基因I(RIG-I)或黑色素瘤分化相关基因5(MDA5),并诱导I型干扰素、白细胞介素-6和其他促炎细胞因子的产生,从而刺激细胞先天免疫的激活。
修饰核苷酸主要是通过阻碍信号受体识别mRNA,避免下游信号通路的激活从而逃避先天免疫反应。Ψ通过阻碍TLR7/8、PKR、OAS和RIG-I介导的信号通路的刺激来降低细胞内先天免疫原性。值得强调的是,这些细胞受体不仅能感知某些修饰的存在与否,还能感知RNA链特征(单链或双链RNA)以及碱基修饰的位置和组合。m5C通过阻止TLR7/8,PKR和RIG-1介导的信号通路的的刺激来降低细胞内先天免疫原性,并稳定mRNA,从而延长半衰期。m6A修饰可降低TLR3/7/8、PKR、MDA5、OAS和RIG-I与mRNA的结合,从而逃避先天免疫。
近岸蛋白mRNA技术-原料/服务一站式解决方案提供包括T7 High Yield RNA Transcription kit (E131) 在内的RNA体外转录所需的多种原料酶和相关辅助试剂,可以满足广大研究者多方面的生产和实验需求。相关产品
|
Cat. No. |
Product Name |
|
E131 |
T7 High Yield RNA Transcription kit |
|
E137 |
T7 High Yield RNA Transcription Kit (N1-Me-Pseudo UTP) |
|
E139 |
T7 High Yield RNA Transcription Kit with CAP1 GAG (3´OMe) |
|
E141 |
T7 High Yield RNA Transcription Kit with CAP1 GAG |
|
M062 | Vaccinia Capping Enzyme |
|
M072 |
mRNA Cap 2´-O-Methyltransferase |
|
M082 |
Cap 1 Capping System |
|
M012 |
E. coli Poly(A) Polymerase |
|
E127 |
DNase I |
|
GMP-S023A |
ATP, GMP Grade |
|
GMP-S026A |
UTP, GMP Grade |
|
GMP-S025A | CTP, GMP Grade |
|
GMP-S024A |
GTP, GMP Grade |
|
GMP-S042 |
N1-Me-Pseudo UTP, GMP Grade |
|
GMP-S048 |
Pseudo UTP, GMP Grade |
|
MR008 |
eGFP mRNA |
|
MR010 |
eGFP mRNA(N1-Me-Pseudo UTP) |
|
MR009 |
Luciferase mRNA |
|
MR011 |
Firefly Luciferase mRNA (N1-Me-Pseudo UTP) |
|
MR016 |
hEPO mRNA (N1-Me-Pseudo UTP) |
|
MR015 | OVA mRNA (N1-Me-Pseudo UTP) |
|
MR105 |
mCherry mRNA(N1-Me-Pseudo UTP) |
|
MR201 |
eGFP circRNA |
|
MR202 |
Luciferase circRNA |
|
MR019 |
Cas9 mRNA (N1-Me-Pseudo UTP) |
|
MR107 |
Cas9 mRNA |
参考文献:
1 Wadhwa A, Aljabbari A, Lokras A, Foged C, Thakur A. (2020) Opportunities and Challenges in the Delivery of mRNA-based Vaccines. Pharmaceutics. Jan 28;12(2):102. 2 Chen Y, Guo D. (2016) Molecular mechanisms of coronavirus RNA capping and methylation. Virol Sin. Feb;31(1):3-11. 3 Muttach F, Muthmann N, Rentmeister A. (2017) Synthetic mRNA capping. Beilstein J Org Chem. Dec 20;13:2819-2832. 4 Cui L, Ma R, Cai J, Guo C, Chen Z, Yao L, Wang Y, Fan R, Wang X, Shi Y. (2022) RNA modifications: importance in immune cell biology and related diseases. Signal Transduct Target Ther. Sep 22;7(1):334.