推荐产品

NovoScript® Plus All-in-one 1st Strand cDNA Synthesis SuperMix (gDNA Purge)
品牌:近岸蛋白(Novoprotein)
询价
询价公司新闻/正文
mRNA加帽率检测伴侣——RNase H
人阅读 发布时间:2023-04-01 11:20
3月22日,石药集团新冠mRNA疫苗的获批,极大地振奋了国内mRNA行业人的信心,mRNA疫苗在国内落地对整个领域的发展具有重要意义。随着mRNA的不断发展,国内外针对其质量控制的要求也越来越严格,产品开发终端的质量控制研究方法也越来越完善。为规范和指导mRNA质量,早在2020年,中国药监局就发布了《新型冠状病毒预防用mRNA疫苗药学研究技术指导原则(试行)》,用以指导mRNA疫苗的生产和质控。2022年2月23日美国药典(USP)也发布了关于“mRNA疫苗质量分析方法”的指南草案。同年5月我国药监局发布了《体外基因修饰系统药学研究与评价技术指导原则(试行)》用于强化mRNA类药品的质量标准。这些指导原则明确对mRNA不同区域结构的完整性提出要求,如5‘-Cap帽或帽类似物结构、poly(A)长度及分布等。
在体外转录获得的mRNA中,加帽反应可分为两种方式:1)转录后酶法加帽;2)共转录加帽。酶法加帽是利用加帽酶(Cat.No.:GMP-M062, Novoprotein)及2’-O-甲基转移酶(Cat.No.:GMP-M072, Novoprotein)的共同作用完成Cap1的修饰。共转录加帽是利用化学合成的帽类似物,在体外转录的过程中,将帽结构添加到mRNA的5’端。

图1:mRNA的帽结构是由一个7-甲基鸟苷通过一个5′–5′三磷酸酯桥连接到mRNA 链的5′核苷上组成。Cap-0结构由相邻的RNA链通过三种酶的依次反应形成。进一步形成cap-1结构需要2’-O-甲基转移酶的参与,该修饰可以降低RNA在体内引起的细胞先天免疫反应。本图引自Decroly, E., Ferron, F., Lescar, J. et al. (2012). Conventional and unconventional mechanisms for capping viral mRNA. Nat Rev Microbiol 10, 51–65。
无论哪种加帽方式,最终获得的mRNA都必须进行加帽率的检测。比较经典的加帽率检测方式是2016年由诺华生物医学研究所发表在Anal Bioanal Chem杂志的一篇文章“Label-free analysis of mRNA capping efficiency using RNase H probes and LC-MS“,文章中使用一种特殊裂解探针法进行mRNA加帽率分析。通过设计mRNA 5’端互补探针,退火形成RNA/DNA杂合链,利用RNase H在特定位置从mRNA的5'末端切割短序列,并用液相色谱-质谱联用仪(LC-MS)分析获得加帽率。
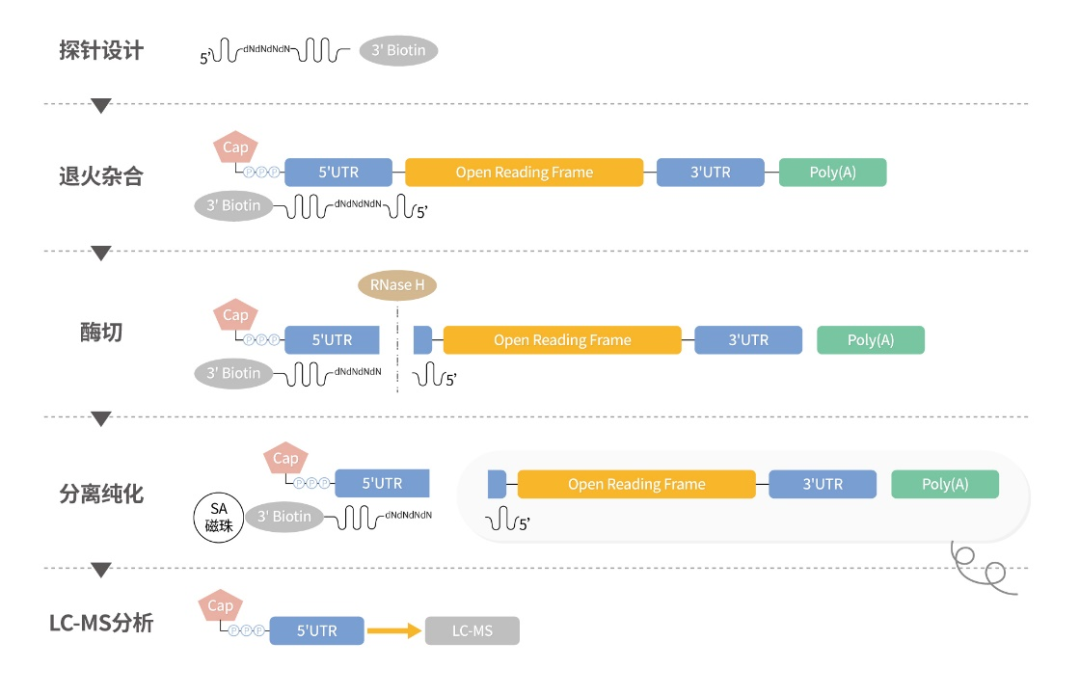
图2:加帽率检测原理
近岸蛋白研发生产的Thermostable RNase H来源于极端嗜热菌Thermus thermophilus,能够在高温的条件下特异性地水解杂交到DNA链上的RNA的磷酸二酯键,故能降解DNA/RNA杂合链中的RNA,而并不消化单链或者双链的DNA。Thermostable RNase H在65℃也能表现出活性,这种特性让该酶能够用于高温实验。近岸蛋白Thermostable RNase H(Cat.No.:E134)经上百例加帽率检测项目验证,可有效酶切获取mRNA 5’端序列,通过LC-MS分析加帽信息。
案例分析:
mRNA样品处理:

将以上混合物混匀后置于PCR仪中,50℃反应45min。
裂解产物经纯化后上机检测:
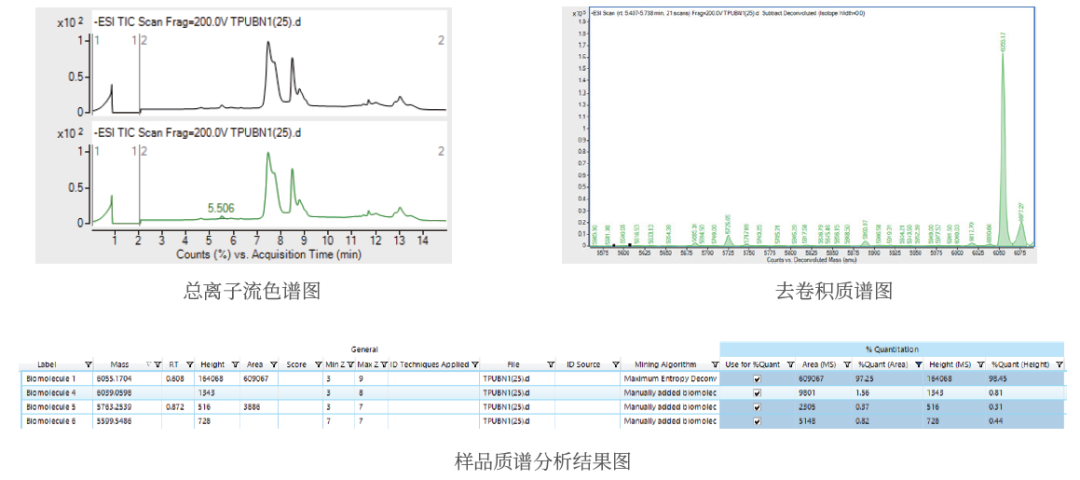
通过以上检测,根据理论分子量在LC-MS结果中匹配对应的Uncapped triphos、Diphos 、G Cap、Cap0、 Cap1成分并计算峰面积占比。
Cap1加帽率=Cap1峰面积占比,Cap加帽率=Cap0峰面积占比+Cap1峰面积占比。
结果示例:
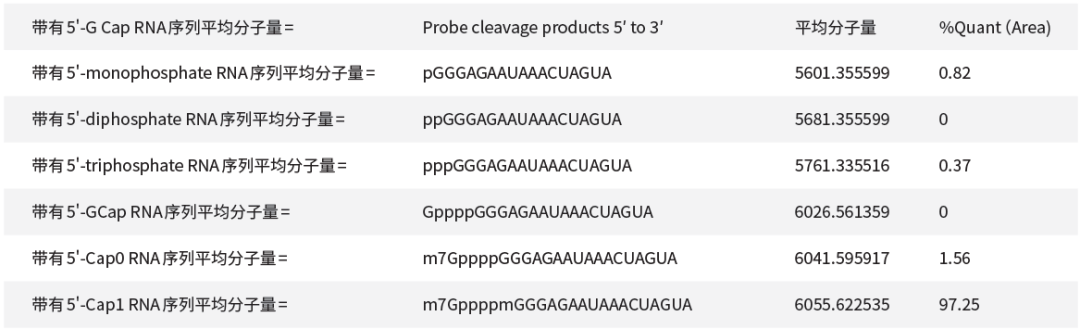
mRNA Cap1加帽效率为97.25% ,Cap0+Cap1 加帽效率为98.81%。
mRNA加帽率检测伴侣——RNase H试用装申领进行时,欢迎扫码申领

近岸蛋白mRNA原料/服务一站式解决方案:
相关产品:
| 目录号 |
产品名称 |
| BspQI, GMP Grade |
|
| 10×BspQI Reaction Buffer, GMP Grade |
|
| XbaI, GMP Grade |
|
| GMP-EB015 |
10×XbaI Reaction Reaction Buffer, GMP Grade |
| BsaI, GMP Grade |
|
| 10×BsaI Reaction Buffer , GMP Grade |
|
| T7 RNA Polymerase, GMP Grade |
|
| 10×Transcription Buffer, GMP Grade |
|
| Vaccinia Capping Enzyme, GMP Grade |
|
| mRNA Cap 2´-O-Methyltransferase, GMP Grade |
|
| 10×Capping Reaction Buffer, GMP Grade |
|
| SAM (32mM), GMP Grade |
|
| E. coli Poly(A) Polymerase, GMP Grade |
|
| 10×Poly(A) Polymerase Buffer, GMP Grade |
|
| Pyrophosphatase, Inorganic (yeast), GMP Grade |
|
| RNase Inhibitor, GMP Grade |
|
| DNase I, GMP Grade |
|
| T7 RNA Transcription Enzyme Mix, GMP Grade |
|
| 10×Transcription Buffer, GMP Grade |
|
| ATP, GMP Grade (100mM) |
|
| ATP, GMP Grade (10mM) |
|
| GTP, GMP Grade (100mM) |
|
| GTP, GMP Grade (10mM) |
|
| CTP, GMP Grade (100mM) |
|
| UTP, GMP Grade (100mM) |
|
| N1-Me-Pseudo UTP, GMP Grade |
|
| Pseudo UTP, GMP Grade |
|
| eGFP mRNA (N1-Me-Pseudo UTP) |
|
| Luciferase mRNA (N1-Me-Pseudo UTP) |
|
| eGFP mRNA |
|
| Luciferase mRNA |
|
| T7 High Yield RNA Transcription kit |
|
| Thermostable T7 RNA Polymerase |
|
| Cap 1 Capping System |
|
| RNA Clean Beads |
|
| Lithium Chloride Precipitation Solution |
|
| Thermostable RNase H |